La falta de sincronía entre los estímulos ambientales o externos y el reloj interno de las células tiene impactos en la salud.

Durante muchos años se había afirmado que la alimentación alta en grasas e hidratos de carbono, así como el sedentarismo eran las causas principales de la obesidad. Sin embargo, nuevas investigaciones han revelado otros factores que contribuyen al desarrollo de trastornos en la función metabólica, uno de ellos es la perturbación de los ritmos biológicos.
Lucía Mendoza Viveros, doctora en Biología Celular y de Sistemas por la Universidad de Toronto, mencionó que la prevalencia de sobrepeso y obesidad, a causa de la dieta y el estilo de vida contemporáneo ha aumentado en la población en las últimas décadas. Datos recientes indican que más de 30% de los adultos en México padecen obesidad, lo cual aumenta el riesgo de padecer enfermedades cardiovasculares, diabetes tipo 2 y trastornos metabólicos.

La investigadora que se hizo acreedora a una de las Becas para las Mujeres en la Ciencia L’Oréal-UNESCO-AMC 2019, señaló que la ritmicidad diaria en la conducta y los procesos fisiológicos de los organismos están regulados por el sistema circadiano, el cual es una adaptación evolutiva de los organismos al ciclo de 24 horas de luz y oscuridad por la rotación de la Tierra, lo que les permite ajustar conductas y funciones de acuerdo con el momento del día en el que se encuentren.
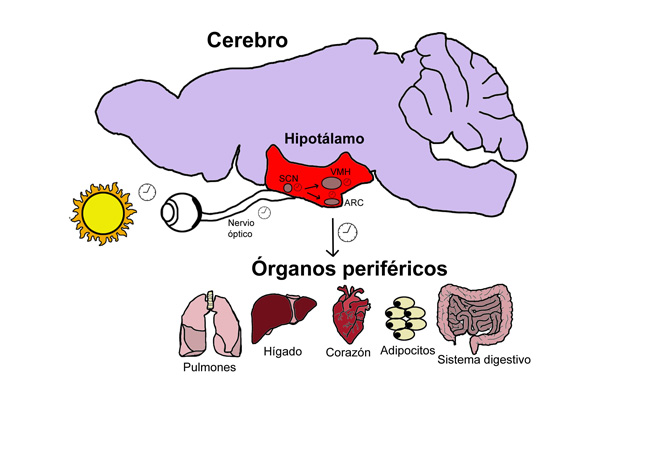
En los mamíferos el sistema circadiano está conformado por un “reloj maestro”, ubicado en el núcleo supraquiasmático del hipotálamo, encargado de mantener las oscilaciones de 24 horas y sincronizarlas con claves externas, principalmente, con el ciclo del día y la noche; así como un “reloj molecular” ubicado en las células y que regula distintos procesos fisiológicos.
La falta de sincronía entre los estímulos ambientales o externos y el reloj interno de las células perturba al sistema circadiano, lo cual tiene impactos en la salud, tal es el caso de las deficiencias en las respuestas metabólicas, la propensión a la obesidad y el síndrome metabólico. Un ejemplo de lo anterior es que cuando ocurre una interrupción crónica de los ciclos de sueño-vigilia en los humanos, disminuye la tolerancia a la glucosa y la respuesta a la insulina.
Por otro lado, una dieta alta en grasas afecta varios aspectos del sistema circadiano, pero con una intervención cronoterapéutica, como restringir la alimentación al periodo más activo del organismo, es posible protegerlo contra la obesidad inducida por una dieta de este tipo.
Y aunque se sabe que el metabolismo —conjunto de funciones que regulan la obtención de energía— está controlado por el sistema circadiano, se desconocen los mecanismos por los que la maquinaria del reloj principal, ubicado en el núcleo supraquiasmático del hipotálamo, regula la ritmicidad en la función metabólica.
Otro aspecto del que falta información, dijo la investigadora, es cómo afecta la alimentación alta en grasas a estos relojes hipotalámicos y por ende a la integración y respuesta a estímulos nutricionales. Por lo que con el proyecto “Relojes hipotalámicos en el control central del metabolismo”, la doctora busca responder a estas preguntas en modelos murinos (roedores).
A estos animales se les da un seguimiento de ganancia de peso y consumo de alimento, esto bajo una dieta estándar o balanceada en comparación con una dieta alta en grasas. Además, se les realizan pruebas fisiológicas, como la tolerancia a la glucosa y a la insulina; se hace un registro de su temperatura a diferentes horas del día, así como de su actividad locomotriz y su conducta alimenticia, detalló la científica.
“Este proyecto busca explorar el papel del reloj molecular en distintas poblaciones neuronales del hipotálamo que controlan el apetito, y el gasto energético, así como en los astrocitos, ya que estas células expresan receptores y responden a señales como la leptina (hormona reguladora del apetito), insulina (hormona que interviene en el aprovechamiento metabólico de nutrientes) y la ghrelina (péptido modulador del metabolismo energético y con efecto estimulador de la ingesta)”.
Además, los astrocitos participan en el metabolismo de ácidos grasos en el cerebro, y son importantes para la respuesta inflamatoria del mismo ante una dieta alta en grasas, continuó la investigadora.
Al respecto del proyecto, la maestra en Ciencias Bioquímicas por la UNAM, señaló que este tiene varias etapas, cada una con diferente grado de avance. “En la primera parte usamos una intervención cronoterapéutica para disminuir los efectos de la dieta alta en grasas, la cual consiste en impedir el acceso al alimento cuando los animales están en su fase menos activa (durante el día, ya que son nocturnos)”.
Después la doctora y su equipo de trabajo analizaron el transcriptoma (análisis masivo de la expresión de genes) del tejido adiposo pardo (que guarda grasas y se encarga de utilizarlas para generar calor) a lo largo del día. Lo que identificaron es que los genes que se expresan con patrones cíclicos en el tejido adiposo pardo de los animales obesos son menos que en los animales sanos.
Mientras que en los animales que recibieron cronoterapia, que pesan más que los roedores sanos pero menos que los obesos, se restaura en gran medida el patrón de expresión de genes a lo largo del día.
“Ahora estamos analizando cuáles son las funciones de los genes que se expresan de manera cíclica y cómo se traduce en la función de este tejido, además de relacionar esta información con el transcriptoma de una parte del cerebro que se encarga, entre otras cosas, de controlar la actividad del tejido adiposo pardo”.
Lucía Mendoza Viveros dijo que la relevancia de este proyecto radica en que puede contribuir a establecer, en un modelo animal, cómo se relacionan los relojes biológicos del hipotálamo con el metabolismo. Y en un futuro se podrán analizar el cambio en el funcionamiento de los órganos periféricos a lo largo del día en distintas condiciones de alimentación y cuáles genes o moléculas están cambiando su función, lo que podría llegar a traducirse, a largo plazo, en blancos terapéuticos.
Foto 1 Portada: En el hipotálamo se encuentra el “reloj maestro” o el núcleo supraquiasmático, el cual recibe información de la retina acerca de la hora del día, para después comunicárselo a los otros núcleos como el ventromedial y arcuato, que organizan la temporalidad del funcionamiento del corazón, hígado, pulmones, adipocitos y sistema digestivo.
Imagen: Cortesía de la investigadora.
Foto 2: Lucía Mendoza Viveros, ganadora de una de las Becas para las Mujeres en la Ciencia L’Oréal-UNESCO-AMC 2019.
Foto: Elizabeth Ruiz/AMC







