

Por Rosario Vega * ambientalnews.mx

@chayito09
Hace tiempo quería contarles una historia muy especial y de la cual me siento muy orgullosa. Por casualidad o por causalidad trabajé en un proyecto maravilloso, que resume todo por lo que estudié químico-biólogo y seguí el camino de la investigación.
Todos quienes trabajamos en ciencia tenemos una meta principal: aportar un granito de arena para ayudar, contribuir con algo para el bien de la humanidad.
Para comenzar, debo contar que trabajo en una pequeña empresa privada de investigación y desarrollo, donde diseñamos y producimos anticuerpos monoclonales y antígenos recombinantes, así como diferentes servicios de análisis de moléculas para el diagnóstico de enfermedades infecciosas, como VIH, malaria, hepatitis B, cólera, sífilis, COVID, etc.

En nuestra empresa hemos tenido la suerte de trabajar con Merck, PALL, el Instituto Pasteur, Lonza, Sartorius, FIND, Medix y Sanofi, entre otros.
Regresando al tema, al momento de ese proyecto éramos cuatro personas en el laboratorio: N, W, S y yo.
N y S trabajaban con Antígenos recombinantes; W era el encargado de dirigir y coordinar todos los proyectos, y yo soy encargada de Anticuerpos monoclonales y análisis de moléculas.
Un buen día, en 2018, mi jefa D recibió una llamada diciéndole que la Organización Mundial de la Salud (OMS) y FIND (The Foundation for Innovative New Diagnostics) (https://finddx.org) estaban en busca de antígenos de malaria y habían realizado lo que podríamos llamar ‘un concurso’, porque necesitaban una referencia mundial. Hay varios en el mercado, pero querían encontrar los mejores en costo/calidad.


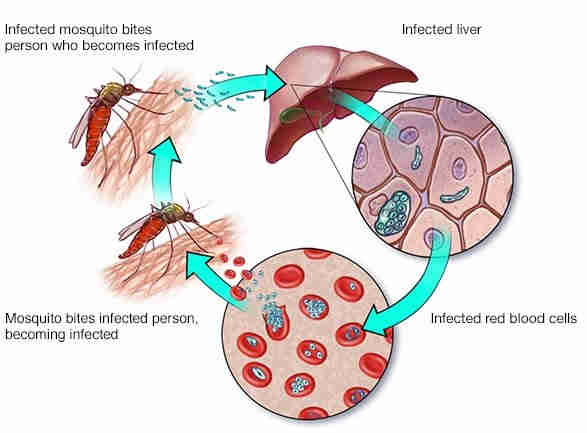
Debemos recordar que la malaria (mejor conocida como paludismo) es una enfermedad potencialmente mortal, causada por parásitos que se transmiten por la picadura del mosco Anopheles y es la mayor causa de muertes en el mundo.
Para entonces, nosotros teníamos dos antígenos de malaria (de la enzima pLDH): Plasmodium falciparum y Plasmodium vivax. Mi jefa contactó a la persona encargada del concurso y mandó nuestros dos antígenos para su evaluación.

Hay que mencionar que había laboratorios de todo el mundo y competíamos contra los mejores, que eran los alemanes.
Tiempo después, D fue llamada a una junta, donde se le dio la noticia de que nuestros antígenos habían sido los mejores en relación calidad/costo. ¡Sí! ¡Mejores que los alemanes! Inmediatamente nos convocó a reunión: tenía que darnos varias noticias.
La primera fue que habíamos ganado. ¡Yei! Peeeeeero -siempre hay un pero-, la OMS no quería solamente dos; quería los antígenos pLDH de las seis especies de Plasmodium… y -siempre hay un y- que estuvieran liofilizados. Todos… T-O-D-O-S. Además, teníamos un año completito para hacerlo. ¡Ajá, como si fuera mucho tiempo para semejante proyecto! Eso sí, que no nos preocupáramos por el dinero: FIND y la OMS iban a financiar.

Para que se den una idea, hay seis especies importantes de malaria: Plasmodium falciparum, P. vivax, P. malarie, P. ovale curtisii, P. ovale walikeri y P. knowlesi. El problema es que su secuencia genética es muy parecida y para hacer un antígeno que sea reconocido en diagnóstico, tenemos que ver que no haya reacción cruzada. Es decir, que el antígeno preparado no reaccione con otro de la misma especie.
A cada uno se nos asignó una parte del proyecto. N, como es el biólogo molecular, tenía que encontrar la secuencia genética de cada antígeno, hacer el plásmido y revisar las condiciones de clonación; S tenía que comenzar a revisar todo lo que tenía que ver con la producción: medio de cultivo, protocolos, etc.
W se encargaría de buscar todo lo referente a la liofilización, desde buffers de almacenamiento hasta el mismo liofilizador, que todavía no desarrollábamos.
Yo me encargaría de la caracterización de los antígenos: encontrar el punto isoeléctrico de cada antígeno, pruebas de ELISA para evaluar la especificidad de cada uno y encontrar anticuerpos específicos para los seis antígenos: que reconociera a todos al mismo tiempo, lo que se conoce como un pan-anticuerpo.


Para los que no sepan lo que es una pruebal de ELISA (acrónimo del inglés Enzyme-Linked Immuno Sorbent Assay / ‘ensayo por inmunoabsorción ligado a enzimas’). Es un procedimiento rutinario y sencillo, compuesto por diferentes pasos y muchas variables: hay que seleccionar los reactivos, la temperatura, los volúmenes, el tiempo de incubación -deben ser muy precisos, ya que el mínimo cambio afecta los pasos sucesivos y el resultado de la prueba-.
Tenía que estandarizar la técnica para todas las especies y encontrar un anticuerpo que reconociera a todas. El problema comenzó cuando, al tratar de estandarizar el protocolo de ELISA, los resultados variaban de una prueba a otra… Intentamos cambiando variables… y nada. Frustrados, comenzamos a revisar y, entre nuestras joyas sin utilizar, teníamos algunos anticuerpos monoclonales que habíamos producido contra Plasmodium pLDH. Comenzamos a descongelar células y revisar su capacidad de reconocimiento con los antígenos que ya teníamos.
Había un hibridoma que era buenísimo y ¡manos a la obra!, lo producimos y caracterizamos. ¡Cuál fue la sorpresa que, al tener todos los antígenos, el mismo anticuerpo reconocía a todos. Fue día de fiesta!
Así seguimos trabajando entre todos. Surgían problemas de improviso (como es normal en ciencia). Por ejemplo, perdimos un mes tratando de encontrar la causa de que nuestras pruebas de ELISA fueran negativas… ¡Sí, todos los ensayos que hicimos durante un mes no sirvieron! Cambiamos antígenos (lotes diferentes), anticuerpos secundarios y, al final, al hacer un recuento, lo que había cambiado era un compuesto de un buffer y ¡voilà!, encontramos la fuente del problema.
Al final de la producción y caracterización de los seis antígenos había que liofilizarlos, es decir quitarles el agua y dejar un polvito con todas las características del antígeno original.
Para los ensayos de liofilización se probaron siete buffers diferentes, cuatro temperaturas (4°C, 37°C, 50°C y -20°C) y todo multiplicado por seis. Debo mencionar que también había que hacer todos los análisis para esas combinaciones. ¡Fue un trabajo monumental!


Al final, todo fue para bien. No podíamos estar más felices porque la OMS y FIND validaron todos los antígenos y puedo decir, con todo orgullo, que somos referente mundial en antígenos pLDH de malaria.
¡Y lo más importante! Estamos apoyando para que menos personas mueran por una enfermedad tan importante en el mundo, ya que nuestros productos se utilizan para diagnosticar la malaria.
Es por eso que si hay un sueño que he cumplido, aunque sea indirectamente, es haber trabajado para la OMS y me llena de orgullo saber que aporté un granito de arena para mejorar este mundo. Fue un gran trabajo en equipo y lo volvería a hacer con muchas ganas y entusiasmo. De hecho, seguimos haciendo análisis para la OMS y FIND.


Ah, y ya para terminar, déjenme contarles que los Centros para el Control y la Prevención de Enfermedades de los Estados Unidos (CDC) serán nuestros clientes.
Agradezco su lectura de algo personal, pero que les comparto con mucho cariño.
* Química-bióloga, MSc Inmunología.







